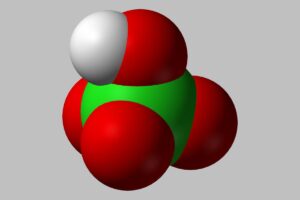
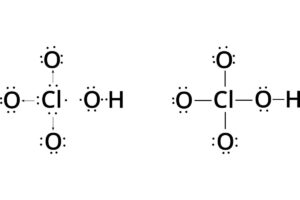
El ácido perclórico es una sustancia muy corrosiva, llegando a ser incluso más fuerte que el ácido sulfúrico, conocido precisamente por su potencia. Los usos del ácido perclórico son muchos, sin embargo destaca su utilidad en la industria armamentística y la ciencia.
Usos del ácido perclórico
El ácido perclórico posee mucha utilidad. Sin embargo, debido a su inflamabilidad, el mismo es más utilizado en la industria.
USOS DEL ÁCIDO PERCLÓRICO. Foto de National Cancer Institute. Unsplash
El ácido perclórico en el área científica
El ácido perclórico suele ser muy utilizado para fines científicos. Diversos productos químicos, e inclusive electrónicos y eléctricos, pueden ser desarrollados en su totalidad con la utilización de este ácido.
El ácido perclórico es muy corrosivo, es decir, es un químico que puede llegar a destruir alguna sustancia o elemento. Es por ello, que también se utiliza para quitar por completo el oxido de los metales.
Por otro lado, muchos percloratos (sales del ácido perclórico) son de gran utilidad para las áreas de estudio. Estos son creados a partir del ácido perclórico, por lo que resulta de gran utilidad.
Usos del ácido perclórico en el hogar
Muchos de los productos de limpieza como desinfectantes, limpiadores profundos, removedores de grasa, entre otros; poseen entre sus componentes un poco de ácido perclórico. Este al ser un ácido tan fuerte, ofrece mejores resultados en los productos de limpieza que se añaden.
Por otro lado, debido a las propiedades del ácido perclórico, también se utiliza para la fabricación de pilas y baterías. Estas son muy útiles en el día a día del hogar, por lo que es otro de los importantes usos del ácido perclórico.
Utilidad en la fotografía
Los usos del ácido perclórico se extienden hasta en la fotografía. En los estudios de revelación, se suele utilizar el ácido perclórico como componente de algún producto útil para la revelación de fotos.
Aunque su uso no es lo común, ya que se suelen utilizar otros ácidos para ello.
Usos en la industria de metales
En la industria de los metales el ácido perclórico suele ser muy utilizado. Casos como la refinación de metales, remoción de óxido, limpieza general, entre otros; son algunos de los principales usos que se le da a este ácido.
Usos del ácido perclórico en la industria armamentística
El uso del ácido perclórico en el sector armamentístico ha venido en aumento. Su utilidad en la fabricación de perclorato de amonio puro, ha sido el detonante de su popularidad. Este perclorato se utiliza para la creación de los explosivos que se suelen usar en los cohetes o misiles.
Muchos instrumentos como balas, municiones, entre otros, son creados utilizando ácido perclórico. Y es que el alto nivel de corrosión y la explosividad que posee, lo hace un químico muy importante para este sector industrial.
Utilidad en la industria farmacéutica
Los percloratos son creados a partir del ácido perclórico. En el caso del perclorato de potasio, es un compuesto muy utilizado en la creación de fármacos antitiroideos. Siendo estos el principal tratamiento en contra del hipertiroidismo.
En vista de que la creación del perclorato de potasio es producto del ácido perclórico. Este ácido resulta esencial para ello.
Otros usos del ácido perclórico
El ácido perclórico es muy utilizado en la industria. Usos como plomería, refinación de metales, entre otros; son actividades en las que suelen utilizar este ácido.
Además, este ácido también se utiliza en el hogar como blanqueador, y algunas veces, como reactivo en la ciencia, con la finalidad de realizar algunos análisis e investigaciones.
Sin duda alguna este ácido posee mucha utilidad en diversos sectores. Sin embargo se debe tener especial cuidado en su manipulación, ya que es altamente explosivo y corrosivo. Por lo tanto, se deben aplicar ciertas medidas de seguridad, implementos, y otros; a fin de mantenerse protegidos tras su uso. Así como también debe ser resguardado con las condiciones requeridas, a fin de evitar explosiones.